【東京薬科大学】尿酸降下薬アロプリノールの作用機序の詳細が明らかに -- 副作用の少ない新たな投与計画の最適化に期待 --
2023年8月29日(火)20時5分 Digital PR Platform
東京薬科大学薬学部病態生理学教室 関根舞助教、市田公美名誉教授(前教授)は、東京大学大学院農学生命科学研究科永田宏次教授、岡本研特任研究員、トロント大学Emil F. Pai教授、カリフォルニア大学Russ Hille教授、日本医科大学西野武士名誉教授との共同研究を行い、尿酸降下薬アロプリノールとその活性代謝物であるオキシプリノールのキサンチン酸化還元酵素(XOR)阻害機構及びその効力には大きな違いがあることを見出し、“アロプリノールの尿酸降下作用の主体はオキシプリノールである”という従来の定説が誤っていることを明らかにしました。これにより、患者へのより適切な尿酸降下療法の提供が期待されます。
【ポイント】
■(成果について)オキシプリノールのXOR(キサンチン脱水素酵素及びキサンチン酸化酵素の総称)阻害機構を高尿酸血症モデルマウス解析、反応速度論解析、X線結晶解析にて詳細に解明しました。
■(研究の背景)アロプリノールは、尿酸への代謝酵素であるXORを阻害することで尿酸生成量を減らし、血清尿酸値を下げます。アロプリノールは代謝されると大部分がオキシプリノールに変換されます。オキシプリノールもXOR阻害効果をもちますが、その阻害機構は同じであり効果の主体と考えられていました。
■(今後の展望)アロプリノール投与方法の最適化による尿酸生成抑制効果の向上と副作用軽減に貢献することが期待されます。
【概 要】
キサンチン酸化還元酵素(XOR)阻害薬であるアロプリノールは半世紀以上の使用実績があり、より強い阻害効果をもつフェブキソスタット、トピロキソスタットが登場した現在でも世界中で広く使用されています。アロプリノールは比較的安全性の高い薬ですが、腎排泄性であることから腎機能障害では減量が必要となるなど、現在でもその有効な投与量について議論されています。開発当初は2~3回に分けての服用が推奨されていましたが、最近では単回投与の使用もみられ、フェブキソスタットとの臨床比較試験においても、比較が容易であることから単回投与が選択されています。このような投与法の背景には、アロプリノールの主代謝物であるオキシプリノールがXOR阻害のエフェクターであり、アロプリノールと同等の阻害効果を発揮するという仮定があります。オキシプリノールは血中半減期が18〜30時間と長く、アロプリノール(血中半減期1~2時間)に比べて血中に蓄積しやすいことから、尿酸降下効果の主体であると考えられています。しかし、明確な根拠は提示されていません。また、欧米諸国では多くの患者が目標血清尿酸値を達成できず800-900 mgまで用量を増やすことが承認されており、これによりスティーブンス・ジョンソン症候群などの重篤な副作用のリスクが懸念されています。副作用の発現にはオキシプリノールの関与が示唆されています。
本研究メンバーはこれまで高尿酸血症・痛風治療薬の標的であるXORの反応機構解析、その阻害薬であるフェブキソスタット、トピロキソスタットの阻害機構解析により、認可・使用までの橋渡し研究を行なってきました(1-4)。そこで得た知見を生かし、高尿酸血症モデルマウス及び新鮮な牛乳(日本獣医生命科学大学付属 富士アニマルファームより提供)から精製したXORを用いた詳細な阻害解析により、今回オキシプリノールの機構解明に取り組みました。
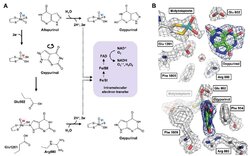
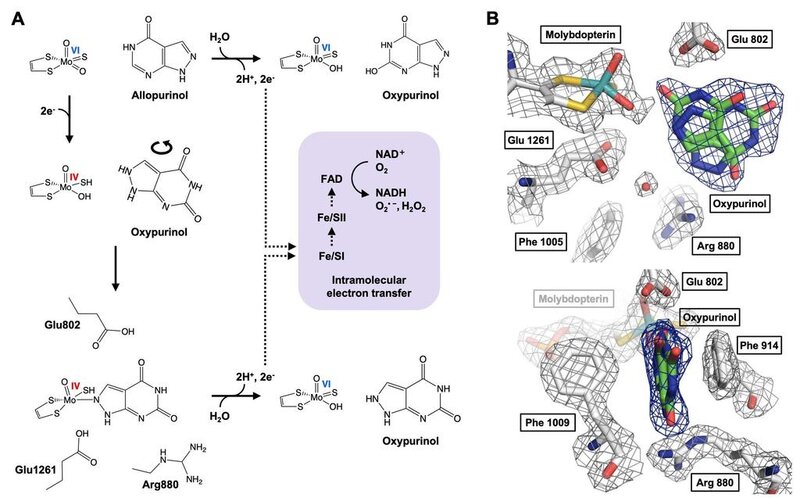
オキシプリノールを高尿酸血症モデルマウスに直接投与すると、アロプリノールよりも弱い尿酸降下作用が得られます。XORが触媒するアロプリノールからオキシプリノールへの反応は、酵素活性部位でのオキシプリノールの回転とモリブデンMo(VI)活性中心のMo(IV)への還元をもたらし、強固な配位結合の形成と尿酸生成抑制効果をもたらします(図1A)。私たちはオキシプリノールの尿酸降下作用の速度論的解析と構造解析を行い、Mo(VI)へ再酸化されるとオキシプリノールの結合は大きく弱まり(図1B)、阻害剤-酵素複合体の再構築にはヒポキサンチン、キサンチン、アロプリノールによる還元が必要であることを示しました。また、XORが触媒する二段階反応(ヒポキサンチン→キサンチン→尿酸)に対し、オキシプリノールはヒポキサンチンからキサンチンへの変換を弱く阻害するだけで、プリン新規合成をフィードバック阻害する可能性が低いことが示されました。さらに、オキシプリノールによるプリンヌクレオシドホスホリラーゼ(PNP)の弱いアロステリック阻害が観察されました。PNPの欠損は主にT細胞の機能障害を通して免疫不全を誘発することがわかっています。
これらの結果より、単回投与法では十分な血清尿酸値低下作用を得るためにアロプリノール投与量を増やす必要があり、過剰投与になりやすいということが示唆されました。ヒポキサンチンからの二段階反応を効果的に阻害するためには、少量のアロプリノールを複数回投与することがより効果的であると考えられます。阻害剤-酵素複合体の半減期を考慮すると、このような分割投与は、血清尿酸値を低下させるのに必要なアロプリノールの総量を減少させると同時に、血中オキシプリノールの蓄積を最小限に抑え、副作用のリスクを減少させることが期待されます。
(A) アロプリノールはXORのモリブデン中心でオキシプリノールに変換され、水分子から酸素を受け取る(上)。電子は2つの鉄硫黄クラスターを経由してFADに渡り、NAD+ (XDH)またはO2 (XO)を還元する。反応の過程でモリブデンは、基質としてのプリン、すなわちアロプリノール(中)から電子を受け取ることによって、Mo(VI)からMo(IV)に還元される。こうして形成されたMo(IV)は一過性にしか生じないが、オキシプリノールが適切に配向すると、阻害剤-酵素複合体を形成する(下)。還元型XOR-オキシプリノール複合体は徐々に再酸化され、オキシプリノールは解離する。(B)遊離のオキシプリノールはモリブデンと明確な結合を示さず、その阻害効果は著しく減弱する。再結合には他の基質(ヒポキサンチン、キサンチン、アロプリノール)が必要である。
本研究成果は日本時間2023年8月23日に米国生化学・分子生物学会の発行するJournal of Biological Chemistryのオンライン版で発表されました。
(1) Hille, R., and Nishino, T. (1995) Flavoprotein structure and mechanism. 4. Xanthine oxidase and xanthine dehydrogenase Faseb j 9, 995-1003
(2) Okamoto, K., Eger, B. T., Nishino, T., Kondo, S., Pai, E. F., & Nishino, T. (2003). An extremely potent inhibitor of xanthine oxidoreductase: crystal structure of the enzyme-inhibitor complex and mechanism of inhibition. Journal of biological chemistry, 278(3), 1848-1855.
(3) Okamoto, K., Matsumoto, K., Hille, R., Eger, B. T., Pai, E. F., & Nishino, T. (2004). The crystal structure of xanthine oxidoreductase during catalysis: implications for reaction mechanism and enzyme inhibition. Proceedings of the National Academy of Sciences, 101(21), 7931-7936.
(4) Okamoto, K., Eger, B. T., Nishino, T., Pai, E. F., and Nishino, T. (2008) Mechanism of inhibition of xanthine oxidoreductase by allopurinol: crystal structure of reduced bovine milk xanthine oxidoreductase bound with oxipurinol Nucleosides Nucleotides Nucleic Acids 27, 888-893.
▼本件に関する問い合わせ先
総務部 広報課
住所:東京都八王子市堀之内1432-1
TEL:0426766711
FAX:042-676-1633
メール:kouhouka@toyaku.ac.jp
【リリース発信元】 大学プレスセンター https://www.u-presscenter.jp/